| Titel: | Unterricht über die Prüfung des Kalk-Chlorüres. (oxidirt salzsaurer Kalk). Von Hrn. Gay-Lussac. |
| Fundstelle: | Band 14, Jahrgang 1824, Nr. CI., S. 423 |
| Download: | XML |
CI.
Unterricht über die Prüfung des
Kalk-Chlorüres. (oxidirt salzsaurer Kalk). Von Hrn. Gay-Lussac.
Aus den Annales de Chemie et de Physique. Junius.
1824. S. 162.
Mit Abbildungen auf Tab.
VIII.
Gay-Lussac's Unterricht über die Prüfung des
Kalk-Chlorüres.
Die Ungewißheit, die bisher in Bestimmung Desjenigen herrschte
was im Handel unter dem Namen Kalk-Chloruͤr
vorkommt, und folglich auch in Bestimmung des Werthes desselben, wodurch seine
Anwendung so sehr vermindert wurde, hat uns veranlaßt einen Unterricht uͤber
dasselbe herauszugeben. Wir wollen diesen in zwei Abschnitte theilen, und in dem
ersten die Grundsaͤze entwikeln, auf welchen die Pruͤfung des
Kalk-Chloruͤres beruht, und in dem zweiten das Instrument beschreiben,
welches wir Chlorometer nennen, und die nothwendigen Handgriffe angeben, um diese
Pruͤfung mit hinlaͤnglicher Genauigkeit fuͤr den Bedarf der
Kuͤnste, die sich derselben bedienen, anzustellen.
I. Abschnitt.
Grundsaͤze, auf welchen die Pruͤfung des Kalk-Chloruͤres
mittelst des Indiges beruht.
Das Chlor zerstoͤrt, wie man weiß, die vegetabilischen Farben, und bildet mit
ihren Grundstoffen neue Zusammensezungen. Um dieser seiner Eigenschaft willen, die
es sowohl im gasfoͤrmigen Zustande, als in Aufloͤsung im Wasser oder
in Verbindung mit einem Alkali besizt, wird es sowohl beim Bleichen als beim Druken
angewendet. Dieselbe Menge Chlores zerstoͤrt in jedem dieser drei Zustande
dieselbe Menge Faͤrbestoffes, und da es, wenn es mit einem Alkali verbunden
ist, Gebundenheit erhaͤlt, beinahe nicht mehr riecht, sich weit besser
aufbewahren und
transportiren laͤßt, auch einen großen Grad von Concentration erhalten kann,
so ist der Vortheil einleuchtend, den man gewinnt, wenn man dasselbe unter dieser
Form bereitet.
Pottasche, Sode und Kalk, im aͤzenden wie im kohlensauren Zustande, verbinden
sich sehr gut mit dem Chlore. Die Verbindung mit der Pottasche, wie sie im Handel
vorkommt, und mit Sode ist in Frankreich seit laͤnger Zeit unter dem Namen
eau de javelle bekannt; die Verbindung mit dem Kalke
hat den Namen oxigenirt kochsalzsaurer Kalk (muriate oxigéne de chaux) erhalten; man
druͤkt sich aber genauer aus, wenn man die erstere, wie es jezt allgemein
geschieht, mit dem Namen Pottasche-Chloruͤr
oder Sode-Chloruͤr, (chlorure de potasse ou de soude), leztere mit den Namen Kalk-Chloruͤr (chlorure de chaux) bezeichnet.
Die Pottasche- Sode- und Kalk-Chloruͤre sind sehr wenig
bestaͤndig; man kann selbst die beiden ersteren nur im fluͤßigen
Zustande mit einer großen Menge Wassers erhalten. Wenn die Pottasche, z.B., sich im
Zustande concentrirter Aufloͤsung befand, und man Chlor in dieselbe gelangen
laͤßt, so bildet sich alsogleich Pottasche-Chloruͤr: dieses
Chloruͤr wuͤrde sich aber durch die Kraft der Aufloͤsbarkeit
großen Theiles bald zersezen, und in chlorsaure Pottasche und Potassium
Chloruͤr umwandeln. Da diese lezteren beiden Verbindungen nicht die
Eigenschaft besizen die Farben zu zerstoͤren, so muß man suchen sie zu
vermeiden, und das einzige Mittel ihrer Bildung zuvorzukommen ist, die Pottasche
sehr verduͤnnt anzuwenden, z.B., hoͤchstens 125 Grammen auf ein Litre
Wasser.
Kalk hat nicht, wie Pottasche oder Sode, die Unbequemlichkeit das Chlor in
Chlor-Saͤure zu verwandelnwerwandeln. Man kann folglich den Kalk in Masse anwenden, um ihn mit dem Chlor zu
verbinden.
Vollkommen trokener Kalk verschlingt has Chlor nicht, verbindet sich aber schnell mit
demselben wenn er im Zustande eines Hydrates ist, d.h., so viel Wasser
enthaͤlt, als er in feuchter Luft aufnehmen kann um zu zerfallen, und sich in
Staub zu verwandeln. Als Hydrat angenommen bildet er, nach Welter, ein basisches Chloruͤr, und uͤberschreitet diesen
Punct nicht. Dieses Sud-Chloruͤr besteht aus
2
Verhaͤltnißzheilen
Kalk
=
2 × 35,603
=
71,206;
2
––––––––––––
Wasser
=
2 × 11,2435
=
22,487;
1
––––––––––––
Chlor
=
––––––––
=
44,2653.
––––––––
137,9583.
Mit Wasser verduͤnnt zersezt es sich alsogleich; die
Haͤlfte Kalkes schlaͤgt sich nieder, und die andere Haͤlfte
bleibt in der Aufloͤsung mit allem Chlor verbunden, und bildet folglich ein
neutrales Chloruͤr.
Es gibt also zwei Verbindungen des Chlores mit dem Kalke, ein
Sub-Chloruͤr und ein neutrales Chloruͤr. Das
Sub-Chloruͤr erhaͤlt man, wenn man das Kalk-Hydrat mit
Chlor saͤttigt, und das Chloruͤr, wenn man das Sub-Chlor im
Wasser aufloͤset, oder den in dieser Fluͤßigkeit verduͤnnten
Kalk mit Chlor saͤttiget.
Das neutrale ChloruͤrChoruͤr, welches wir geradezu Chloruͤr nennen wollen, ist hoͤchst
aufloͤsbar; man kann es jedoch zur Kristallisation bringen, und in kleinen
Prismen erhalten. Seine Aufloͤsung zersezt sich, dem Zutritte der Luft bloß
gestellt, nach und nach; ein Theil des Kalkes verbindet sich mit der in der Luft
enthaltenen Kohlensaͤure, und das mit demselben enthaltene Chlor entwikelt
sich. Man kann diese Zersezung des Chloruͤres dadurch verzoͤgern, daß
man immer uͤberschuͤßischen Kalk in der Aufloͤsung desselben
aufgeloͤst erhaͤlt. Aus diesen Eigenschaften des Chloruͤres
erhellt der Vortheil, den man dadurch erlangt, daß man bloß basisches
Chloruͤr erzeugt; es laͤßt sich als solches viel leichter aufbewahren
und transportiren.
Die Menge Chlores, welche mit dem Wasser oder mit einer Basis verbunden ist,
laͤßt sich auf verschiedene Weise des stimmen: man gab aber in den
Werkstaͤtten, wo die Pruͤfung schnell geschehen muß, dem Verfahren des
Hrn. Descroizilles den Vorzug, welches sich auf die Eigenschaft des Chlores
gruͤndet den Indigo zu entfaͤrben. 1 Theil Indigo in 9 Theilen
concentrirter Schwefelsaͤure aufgeloͤst, und mit 990 Theilen Wasser
verduͤnnt, gibt die gefaͤrbte Fluͤßigkeit, deren man sich
allgemein bedient um den Gehalt des Chlores zu bestimmen.
Unter gleichen Umstaͤnden entfaͤrbt das Kalk-Chloruͤr
eine seiner Menge angemessene Menge dieser Fluͤßigkeit; unter verschiedenen
Umstaͤnden aber erhaͤlt man sehr verschiedene Resultate. So wild, wenn man
Chloruͤr in Indigo gießt, und diese Operation nicht sehr schnell geschieht,
weit weniger Chloruͤr zur Entfaͤrbung noͤthig seyn, als im
entgegengesezten Falle. Das Minimum an Indigo-Aufloͤsung, welches das
Chlor entfaͤrben kann, erhaͤlt man, wenn man sehr langsam den Indigo
in das Chloruͤr gießt, und das Maximum, wenn man gleichfalls sehr langsam das
Chloruͤr in den Indigo schuͤttet. Wiederholte Versuche haben bewiesen,
daß das sicherste Verfahren um bestaͤndig gleichfoͤrmige Wirkungen zu
erhalten, welche man mit Sicherheit vergleichen kann, darin besteht, daß man schnell Indigo-Aufloͤsung in die
Aufloͤsung des Chloruͤr gießt, oder umgekehrt diese in jene. Wir
werden spaͤter die Verfahrungs-Weise angeben.
Wenn der im Handel vorkommende Indigo rein waͤre oder wenn man denselben
wenigstens immer von gleichem Gehalte bekaͤme, so wuͤrde die Menge
seiner Aufloͤsung, die man bei jedem Versuche anwendet, die correspondirende
Menge Chloruͤr anzeigen; da aber der Indigo von sehr verschiedener
Beschaffenheit ist, so kann man die Resultate der Proben mit verschiedenem Indigo
nicht unter einander vergleichen. Um diese Unsicherheiten zu beseitigen, haben wir,
nach dem Beispiele des Hrn. Welter, als Einheit der
entfaͤrbenden Kraft jene Kraft des reinen und trokenen Chlores angewendet,
welche dasselbe unter einem Druke von 0m 76 bei 0° TemperaturAm hundertgraͤdigen Thermometer? aͤussert. Wir nehmen nun. was immer fuͤr einen Indigo, aber
von der besten im Handel vorkommenden Sorte, und bereiten aus demselben eine solche
Aufloͤsung, daß das Chlor genau zehn Mahl sein Volumen entfaͤrbt:
diese Aufloͤsung nennen Wir Probe-Tinctur (teinture
d'épreuve). Grad (degré) nennen wir jedes Volumen der entfaͤrbten Probe-Tinctur und theilen den Grad in 10
Theile.
Wenn man demnach 10 Gramme Kalk-Chloruͤr in Wasser so aufloͤst,
daß man Ein Liter dieser Aufloͤsung erhaͤlt, so zeigt die Zahl der
Volumen Judigs oder der Grade, die von einem Volumen dieser
Chloruͤr-Aufloͤsung zerstoͤrt werden, die Zahl der
Zehntel Litres Chlor, welche diese enthaͤlt. Folglich wird ein Kilogramm
Kall-Chloͤruͤr, dessen Gehalt auf obige Weise bestimmt wurde,
und z.B. 7° 6 oder 76 Centimen waͤre, 76 Litres Chlor enthalten. Jeder
Grad ist also so viel, als 10 Litres in einem Kilogramme Chloruͤr. und jedes
Zehntel 1 Liter. Nimmt man das basische Kalk-Chloruͤr als vollkommen
rein an, und so wie wir es oben angegeben haben, so haͤlt es im Kilogramme
101 Lines, 21 Chlor.
Der Grundsaz, den wir angenommen haben, schien uns seiner Einfachheit und
Bestimmtheit im Ausdruke wegen in der Chlorometrie den Vorzug zu verdienen, er kann
derselbe bleiben, man mag was immer fuͤr ein Mittel zur Messung der
Staͤrke des Chores anwenden.
Man erhaͤlt, im Allgemeinen, eine groͤßere Praͤcision mit einer
schwachen Chlor-Aufloͤsung, die z.B. 4 bis 5 Grade zeigt, als mit
einer sehr gesaͤttigten Aufloͤsung. Wenn man also, bei einem ersten
Versuche, finden sollte, daß das Chloruͤr 10° um Vieles
uͤberstiege, so muͤßte man derselben ein bekanntes Volumen Wasser
zusezen, z.B. zwei Mahl so viel als jenes der Aufloͤsung. Man wuͤrde
hierauf die Pruͤfung vornehmen, und die gefundene Zahl der Grade
verdreifachen, um den wahren Gehalt des Chloruͤres zu finden.
Pruͤfung des Braunstein-Oxides.
Das Braunstein-Oxid, dessen man sich zur Bildung des Chlores bedient, ist von
sehr verschiedener Reinheit, und es ist folglich wichtig den Grad der lezteren zu
kennen.
Hr. Berthier hat seine Analysen mehrerer Arten
Braunstein-Oxides in den Annales de Chemie et de
Physique T. 20. S. 344. (Polytechn. Journ. B. IX. S. 243) bekannt gemacht. Da die Menge
Chlores. welche diese Arten liefern, den Werth derselben bestimmt, so haben wir,
nach diesem Grundsaze, folgende Uebersicht derselben entworfen:
1
Kilogramm
reinen Braunsteines liefert
0 K.
7964
Chlor.
–––––––
Krettnischen
–––
7525
–
–––––––
Calveron (Aude) ohne
Kalkstein
–––
7658
–
–––––––
Calveron, mit Kalkstein
–––
5724
–
–––––––
Périgneux (Dordagne)
–––
5179
–
–––––––
Romanèche (Saone
de Loire)
–––
4692
bis 0,5135
–––––––
Laveline (Vosges)
–––
4648
–
1
Kilogramm
Pesillo (Piémont) schwarz ohne
Kalkstein liefert
0 K.
4426
Chlor.
–––––––
Pesillo mit Kalkstein
–––
3320
–
–––––––
St. Marcel in Piemont
–––
2789
bis 0,3098.
Diese Resultate bestimmen wenigstens annaͤherungsweise den Werth dieser
verschiedenen Arten von Braunstein; um aber den Werth irgend einer Art von
Braunstein zu bestimmen, ist es noͤthig denselben zu pruͤfen, was auf
folgende Weise leicht geschehen kann.
Reines Braunstein-Peroxid besteht
aus
Braunstein
3
Gr.
5578
Sauerstoff
2
–
0000
––
–––
–––––
5
–
5578
und kann 4 gr., 4265 Chlor erzeugen, oder 1 Litt., 3963 bei
einer Temperatur von 0° und unter einem Druke von 0m, 76°; folglich wuͤrden 3 Gr., 980
desselben 1 Litte Chlor, und 1 Kilogramm 251 Litr. 23 Chlor liefern.
Man nimmt also 3 Gr. 980 Braunstein-Oxid von derjenigen Art, die man
pruͤfen will, behandelt sie bei gelinder Hize mit
Hydrochlor-Saͤure, und faͤngt das sich entwikelnde Chlor in
etwas weniger als einem Litre Kalkmilch auf; gegen das Ende der Operation kocht man
die Hydrochlor-Saͤure, um das Chlor aus den Gefaͤßen in die
Kalkmilch uͤbergehen zu machen, und sezt dem Kalk-Chloruͤr so
viel Wasser als noͤthig zu, um das Litte voll zu machen. Der Gehalt dieses
Chloruͤres wird genau den Gehalt des Braunstein-Oxides geben.
Die Guͤte eines Braunstein-Oxides haͤngt nicht bloß von der
Menge Chlor ab, welche dasselbe liefern kann, sondern auch von der Menge
Hydrochlor-Saͤure, die man anwenden muß, um das Chlor zu erzeugen.
Diese Operation ist aber zaͤrtlich, und der niedrige Preis der
Hydrochlor-Saͤure macht sie uͤberfluͤßig. Wir wollen nur
bemerken, daß das Braunstein-Peroxid oͤfters kohlensauren Kalk
enthaͤlt, und Schwerere und Eisen, welche die Hydrochlorsaͤure zum
Theile umsonst zersezen; daß ferner, da der Braunstein nicht immer im Zustande des
Peroxides sich befindet, die Menge Hydrochlorsaͤure, welche er fordert, in
diesem Falle nicht mehr mit der Menge des erhaltenen Chlors in Verbindung steht.
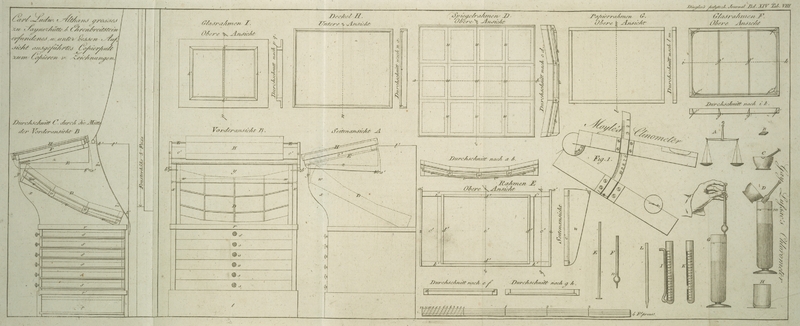
II. Abschnitt. Beschreibung
des Chlorometers und der Verfahrungs-Weise bei Pruͤfung des
Kalk-Chloruͤres.
A, Kleine Wage.
B, Gewicht von 5 Grammen.
C, Moͤrser zum Pulvern des
Kalk-Chloruͤres. Wenn man das Kalk-Chloruͤr
puͤlvert, so ist man eines genaueren Erfolges sicher, indem sich
oͤfters Kluͤmpchen in demselben befinden, die sich nur langsam
aufloͤsen.
D, Gloke mit einem Fuße, die bis zu dem Striche m mit gegenuͤberstehenden Pfeilen, 1/2 Litre
enthaͤlt. Die Oberflaͤche des Wassers muß mit diesem Striche
uͤbereinstimmen, und nicht der obere Rand, der durch die punctirte Linie
angezeigt ist.
E, Ruͤhrer, zum Ruͤhren der
Aufloͤsung des Chloruͤres, und zu gleichfoͤrmiger Verteilung
des lezteren: man stoͤßt und hebt ihn abwechselnd in der Aufloͤsung
auf und nieder, ohne ihn aus derselben herauszuziehen.
E, Kleines Maß oder Pfeifchen von 2 1/2
Kubik-Centimetern, welches bei dem Chlorometern, wovon hier die Rede ist,
immer dasselbe bleiben muß. Es dient zur Messung der Kalk-
Chloruͤr-Aufloͤsung. Um dieses Pfeifchen zu fuͤllen,
senkt man dasselbe bis uͤber den Strich, n, in
das Chloruͤr, durch welchen sein koͤrperlicher Inhalt bestimmt wird,
oder man laͤßt das Chloruͤr in demselben durch Saugen aufsteigen.
Nachdem es sich gefuͤllt hat, legt man den Zeigefinger, der weder zu naß noch
zu troken seyn darf, auf die obere Oeffnung desselben, zieht es aus der
Fluͤßigkeit, und stellt sein unteres Ende auf den Rand der Gloke, wie man in
G, sieht, oder auf den Druk gehoͤrig
anzubringen weiß, und dem Stiele des Maßes zwischen den Fingern eine leichte
abwechselnde kreisfoͤrmige Bewegung zu geben versteht, so senkt sich die
Fluͤßigkeit langsam hinab, und wenn der untere Theil der concaven Linie, der
sie schließt, in der Ebene des kleinen Pfeiles ist, stellt man den Ausfluß dadurch, daß man etwas
staͤrker druͤkt, und leert es in das große Trinkglas HWenn dieses Maß undurchsichtig geworden ist, gibt man demselben seine
Durchscheinenheit dadurch wieder, daß man es in Hydrochlorsaͤure oder
in Eßig taucht. A. d. Ueb. (Es legt sich naͤmlich der fluͤßige
Chlorin-Kalk so fest an das Glas an, daß es seine Durchsichtigkeit
ganz verliert, welche nur durch Anwendung von Saͤuren wieder
hergestellt werden kann. D.).
H, großes Trinkglas zur Mischung der
Probe-Tinctur mit dem Chloruͤr.
Dieses Glas muß auf ein Blatt weißes Papier gestellt werden, indem man auf diese
Weise leichter die Veraͤnderungen, die der Indigo an seiner Farbe durch das
entfaͤrbende Chlor erleidet, bemessen kann.
I, Kaͤnnchen zur Messung der
Probe-Tinctur. Jede groͤssere Abtheilung oder jeder Grad haͤlt
eben so viel Fluͤßigkeit, als das kleine Maß F,
und ist in 5 Theile getheilt, was fuͤr die Anwendung in Fabriken zureicht;
zur Berechnung hingegen muͤssen die Fuͤnftel in Zehntel verwandelt
werden. Man fuͤllt das Kannchen mit der Probe-Tinctur bis auf
0°, was sehr leicht ist; man gießt etwas mehr Probe-Tinctur hinein,
als man braucht, und laͤßt das Ueberfluͤßige, Tropfen fuͤr
Tropfen, durch den Schnabel abfließen, dessen Ende mit einer leichten Lage von Wachs
oder Talg bedekt seyn muß, damit man die Tropfen desto sicherer fallen lassen
kann.
K, eine Roͤhre, die eben so, wie das
Kaͤnnchen, aber in umgekehrter Richtung, in Grade getheilt seyn muß. Sie
dient zur Aufnahme der Probe-Tinctur, die man schnell in die
Chloruͤr-Aufloͤsung schuͤtten muß. Um mit Bequemlichkeit
das noͤthige Volumen der Tinctur zu erhalten, bedient man sich der an ihrem
unteren Ende verduͤnnten Roͤhre L. Man
nimmt das Ueberschuͤßige derselben dadurch weg, daß man die Roͤhre
mehr oder minder tief eintaucht, und mit dem Zeigefinger auf die obere Oeffnung
druͤkt, ehe man sie herauszieht. Was abgehen sollte, ersezt man, indem man
auf dieselbe Weise mit der Roͤhre in der Flasche schoͤpft, welche den
Indigo enthaͤlt.
Bereitung der Indigo-Aufloͤsung und der
Probe-Tinctur mit dieser Aufloͤsung.
Man nimmt eine bestimmte Menge durch ein seidenes Sieb durchgesiebten Indigs, sezt
sie in eine Retorte mit 9 Mahl so viel concentrirter Schwefelsaͤure, und hizt
sie in einem Wasserbade bis zur Siedehize sechs bis acht Stunden lang. Man
verduͤnnt hierauf einen Theil dieser Indigo-Aufloͤsung mit
einer hinlaͤnglichen Menge Wassers, so daß Ein Volumen Chlor genau zehn Mahl
so viel derselben, dem Volumen nach, entfaͤrbt, was dann die
Probe-Tinctur gibt. Die allereinfachste und zugleich hinlaͤnglich
genaue Weise eine Fluͤßigkeit zu bereiten, die ihr Volumen-Chlor
enthaͤlt, ist. 3 Gr. 980 in schoͤnen Nadeln kristallisirtes
Braunstein-Peroxid zu nehmen, dasselbe mit Hydrochlorsaͤure zu
behandeln, das Chlor in Kalk- Milch aufzufangen, und deren Volumen nach der
Operation auf 1 Litre zu reduciren, wie bei der Pruͤfung der
Braunstein-Arten angegeben wurde. Wenn man aber mit aller moͤglichen
Genauigkeiten wollte, muͤßte man das Chlor im gasfoͤrmigen Zustande
bereiten, und dasselbe vom Wasser verschlingen lassen, in welchem etwas Kalk
vertrieben wurde, wobei die Temperatur, der Druk und die Feuchtigkeit desselben in
Rechnung gebracht werden muͤßte.
Wichtige Bemerkung.
Da die Probe-Tinctur nach und nach durch das Licht entfaͤrbt wird, muß
man sie gegen lezteres wohl bewahren, was am besten dadurch geschieht, daß man sie
in steinernen Kruͤgen aufbewahrt. Zum Gebrauche des Chlorometers kann man
sich einer glaͤsernen Flasche von 1/2 Litre bedienen, jedoch mit der
Vorsicht, dieselbe nicht den Sonnenstrahlen auszusezen. Am besten ist es, diese
Flasche in einem Kasten aufzubewahren.
Verfahren bei Pruͤfung des Chloruͤrs.
Man nimmt aus der Masse des zu pruͤfenden ChloruͤresChlouͤres mehrere Muster, und mengt sie, um die mittlere Guͤte desselben zu
erhalten; wiegt 5 Gramme dieser Mischung ab, zerreibt sie in einem Moͤrser
mit einer hinlaͤnglichen Menge Wassers, um daraus eine klare Bruͤhe zu
erhalten, verduͤnnt sie noch mit einer neuen Menge Wassers, und gießt sie in die Gloke
von 1/2 Liter ab. Um diese Operationen ohne Verlust an Fluͤßigkeit zu
vollenden, stuͤzt man den Rand des Moͤrsers gegen den Stoͤssel,
wie die Figur D zeigt. Man zerreibt noch ein Mahl den
Ruͤkstand des Chloruͤres, der im Moͤrser zuruͤk
geblieben seyn mochte, verduͤnnt, gießt ab, und wiederholt diese Operationen
so lang, bis alles Chloruͤr zerrieben ist, und nichts mehr von demselben in
dem Moͤrser zuruͤk bleibt. Man waͤscht diesen aus und gießt das
Wasser in die Gloke. Man ergaͤnzt das Volumen eines halben Line, welches die
Chloruͤr-Aufloͤsung haben muß, schuͤttelt die
Fluͤßigkeit gehoͤrig, um sie vollkommen gleichfoͤrmig zu
machen. Nun fuͤllt man das Kaͤnnchen mit Probe-Tinctur bis auf
o, und gießt aus demselben in das Glas H weniger als man vermuthet, daß durch eine Maße
Chloruͤr entfaͤrbt werden muß, z.B. 5°.
Nun nimmt man mit dem Pfeifchen F eine Maß
Chloruͤr, und laͤßt sie schnell in die Tinctur fließen, indem man in
die Roͤhre blaͤst: waͤhrend dieser Zeit wird die Mischung
geruͤhrt. Wenn die Tinctur vollkommen entfaͤrbt wurde, so sezt man
alsogleich aus dem Kaͤnnchen soviel zu, als noͤthig ist um diese
Fluͤßigkeit etwas gruͤnlich zu faͤrben. Die Menge dieser
Probe- Tinctur, welche in dem Kaͤnnchen fehlt, wird das Maß des
Inhaltes des Chloruͤres, vorausgesezt, daß die Menge der Tinktur, welche man
zum zweiten Mahle zusezte, nicht sehr bedeutend ist, und nicht drei Zehntel Grad
betraͤgt.
Wenn aber diese zum zweiten Mahle aus dem Kaͤnnchen zugegoßene Menge
Chloruͤres mehr als drei Zehntel Grad betraͤgt, z.B. 1°2, so
muß man den Pruͤfungs-Versuch wieder von vorne beginnen. Man
fuͤllt das Kaͤnnchen mit Tinctur, und gießt eben soviel davon in das
Glas, als in dem vorigen Versuche entfaͤrbt wurde, und selbst noch einige
Hundertel mehr. Man sezt die Operation uͤbrigens auf die oben angegebne Weise
fort. Der Probe-Versuch hat nur dann den hoͤchsten Grad von
Genauigkeit erreicht, deren er faͤhig ist, wenn die Probe-Tinctur
unmittelbar, wie man das Chloruͤr in dieselbe bringt, die angezeigte Farbe
annimmt, ohne daß es nothwendig wird neuerdings Tinctur aus dem Kaͤnnchen
zuzusezen.
Durch diese auf einander folgenden Operationen kommt man dem wahren
Chloruͤr-Gehalte so nahe als moͤglich: indessen glauben wir
nicht, daß man fuͤr mehr als 1/50 uͤberhaupt buͤrgen kann. Das
hier angegebene Verfahren wird vielleicht complicirt erscheinen; wir glauben aber
hier nur bemerken zu muͤssen, daß jede der verschiedenen Operationen in zwei,
drei Minuten vollendet ist; daß, wenn man schon vorher den Gehalt des
Chloruͤres beilaͤufig kennt, zwei Operationen hinreichen; und daß
endlich, zum Fabrik-Gebraͤuche, schon eine einzige Operation
genuͤgt. Wo es sich aber darum handelt, den Gehalt des Kalk,
Chloruͤres mit Genauigkeit zu kennen, damit man den Werth desselben darnach
bestimmen kann, darf man, wie wir vermuthen, weder Zeit noch Sorgfalt sparen.
Dasselbe Verfahren laͤßt sich unmittelbar auf Pruͤfung einer
Chlor-Aufloͤsung in Wasser anwenden; indessen ist es besser, wenn man
damit anfaͤngt, daß man etwas gepulverten lebendigem Kalk zusezt, um dasselbe
in Chloruͤr zu verwandeln. Das sogenannte eau de
javelle, welches gleichfalls ein Chloruͤr ist, wird durchaus auf
dieselbe Weise gepruͤft.
Die Roͤhre k, die zu dem Chlorometer
gehoͤrt, dient zur Pruͤfung des Chloruͤres, indem man schnell
den Indig in das Chloruͤr gießt. In dieser Hinsicht sucht man zuerst mit dem
Kaͤnnchen, wie viel man Tinctur braucht, um eine Maß Chloruͤre zu
saͤttigen.
Man faͤngt den Versuch damit wieder an, daß man in die Roͤhre k eben so viel Tinctur bringt, als entfaͤrbt
wurde, und selbst noch etwas mehr, und gießt sie schnell in eine neue Maß
Chloruͤr; man sezt noch soviel von der Tinctur, als fehlen sollte, zu, um die
gruͤnliche Farbe zu erhalten, und faͤngt den Versuch wieder von vorne
an, indem man in die Roͤhre eben so viel Tinctur bringt, als in dem
vorhergegangenen Versuche entfaͤrbt wurde. Der Gang dieses Verfahrens ist
genau derselbe, wie bei dem ersteren; da aber bei gleichen Resultaten hier noch die
Roͤhre K und das Pfeifchen L noͤthig ist, so glauben wir nicht, daß dasselbe den Vorzug
verdientDiese Pruͤfungsart sezt schon einen gewandten Experimentator voraus.
So wie wir den vom Hrn. Verfasser beschriebenen Apparat aus Paris erhalten,
werden wir von unsern Versuchen, welche wir nach unsern Maßen angeben
werden, nachtraͤglich mittheilen und die geraͤthschafte auf
deutschen Glashuͤtten fuͤr Liebhaber derselben anfertigen
lassen. Ueber diesen Gegenstand vergl. man auch polyt. Journal. B. 4. S. 477. D..
Tafeln